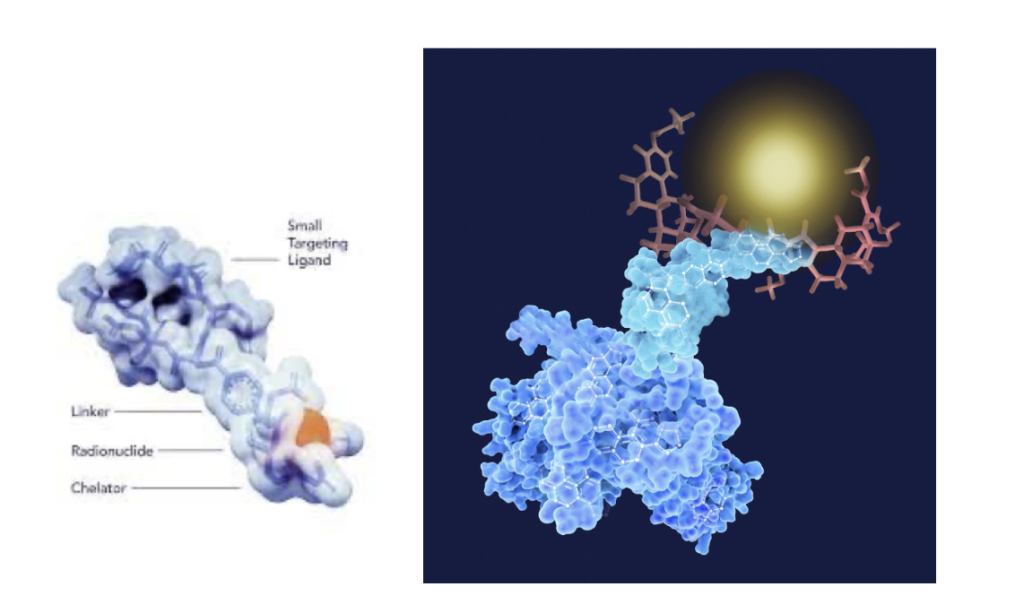
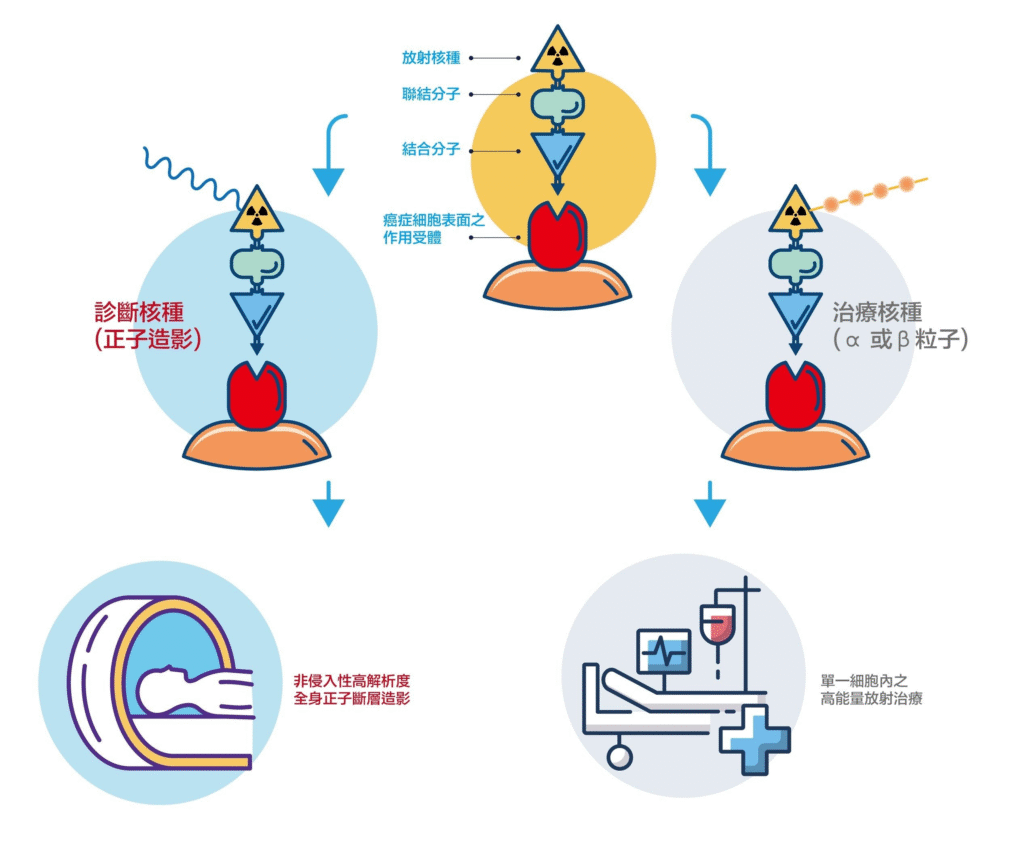
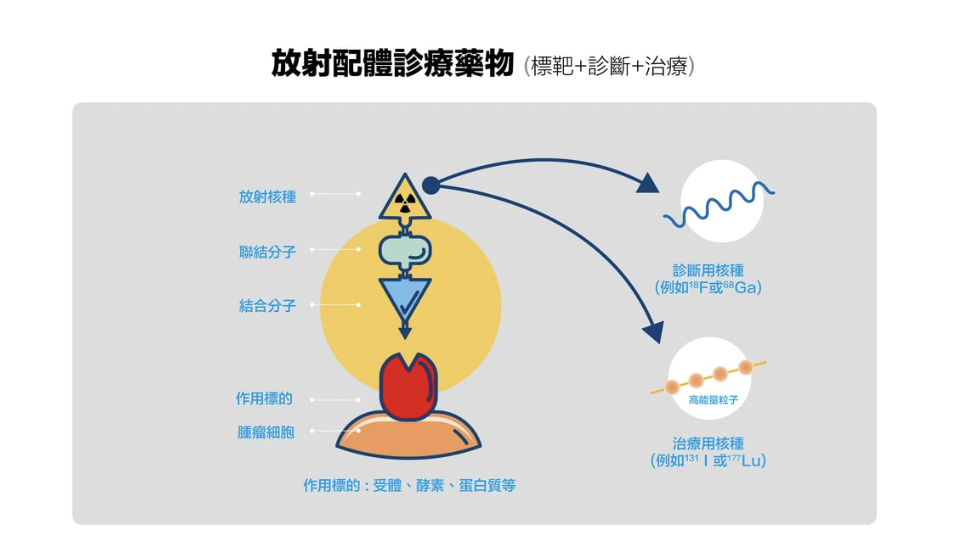
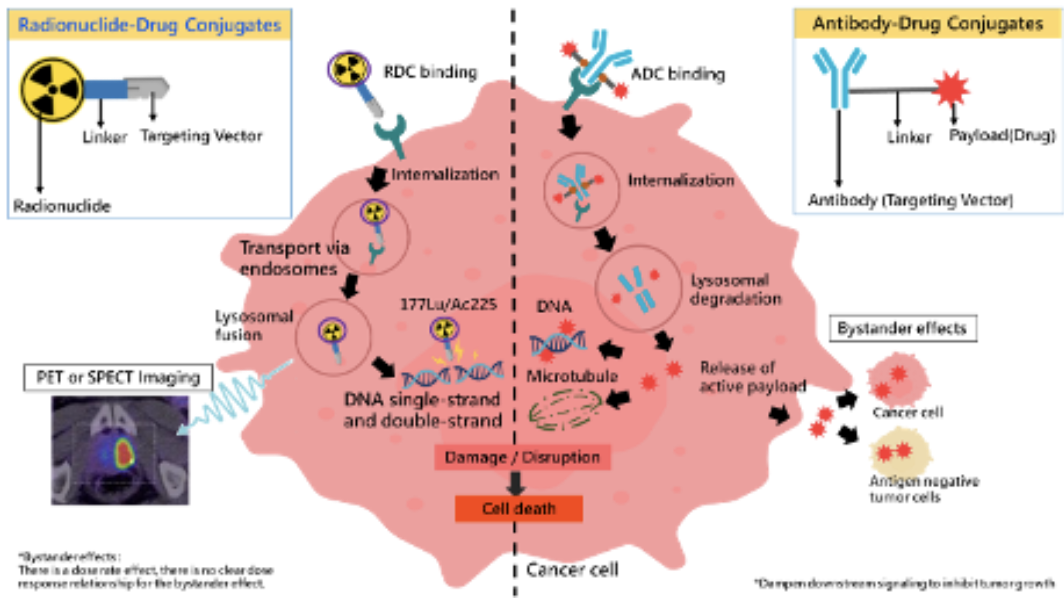
RDC組成結構
-
連結分子 (Linker)
作為靶向分子與放射性核種的橋樑,Linker能調控藥物的代謝與分布。其結構和設計對放射性藥物複合體(RDC)的開發至關重要。普瑞默高度重視Linker的設計與品質,以確保藥物在體內吸收與代謝的穩定性。 -
靶向分子(Target Molecule)
靶向分子可為抗體、小分子或者胜肽,能與特定腫瘤或腫瘤微環境細胞相關的受體、酵素或蛋白質專一結合,賦予藥物對腫瘤細胞高度的專一性與精準的標靶能力。 -
螯合分子(Chelator)
螯合是金屬離子與其他分子的一種鍵合,在配體和中央金屬原子之間形成多重鍵,螯合劑被廣泛應用於新型共軛藥物中,對於連接放射性核素和遞送部分的RDC尤其重要。 -
放射性核種(Radionuclide)
RDC 的治療原理主要仰賴放射性核種釋放的游離輻射來對腫瘤細胞造成破壞